检查点抑制剂的成功是癌症治疗领域一项重大的进步,因为它与化疗或靶向疗法截然不同。PD-1和CTLA-4抗体是癌症免疫疗法中的重要成员,为晚期黑色素瘤患者带来了前所未有的希望,并且在其它癌症类型中也显示出了巨大的潜力。
然而,这种疗法也导致了一些独特的、通常与免疫相关的不良反应(adverse events that are mostly immune-related,irAEs)。患者免疫系统的激活有时会导致严重的、甚至致命的毒副作用。早期识别和管理这些irAEs对临床医生至关重要,这将有助于更加成功、安全的使用这些新型免疫疗法药物。
今年5月,Nature Reviews Clinical Oncology杂志上发表了题为“Safety profiles of anti-CTLA-4 and anti-PD-1 antibodies alone and in combination”的综述文章。作者们概括了靶向PD-1和CTLA-4的检查点抑制剂相关的不良反应,旨在为癌症免疫疗法更好的应用提供一些通用准则。
CTLA-4及PD-1抗体
在过去的十年里,科学家们开发了2个靶向CTLA-4的全人源化单克隆抗体,分别为ipilimumab和 tremelimumab,最初主要是在晚期黑色素瘤患者中进行测试。初步调查中,这两个抗体的响应率是相似的,但在两个随机临床试验中,只有ipilimumab治疗带来了重要的生存益处。
Ipilimumab分别在2011年3月、7月获得了FDA和EMEA的批准,作为单一用药,治疗转移性黑色素瘤。文章表示,ipilimumab和 tremelimumab正被积极开发用于治疗其它类型的癌症,如非小细胞肺癌、前列腺癌和间皮瘤。
值得注意的是,今年2月29日,tremelimumab目前的开发商阿斯利康宣布,该药作为二线或三线疗法治疗不可切除的恶性间皮瘤的IIb期临床试验没能达到总生存期的主要终点(primary endpoint of overall survival)。尽管这一试验宣告失败,但公司认为tremelimumab依然是Immuno-Oncology产品线联合治疗策略中的关键组成部分。
另一种已经成功实现临床转化的免疫检查点是PD-1。目前,有两个PD-1抗体获批,分别为Nivolumab和Pembrolizumab。前者已“拿下”4个适应症,包括黑色素瘤、肺癌、肾癌以及经典型霍奇金淋巴瘤,后者获批的适应症包括黑色素瘤和肺癌。
调节机制
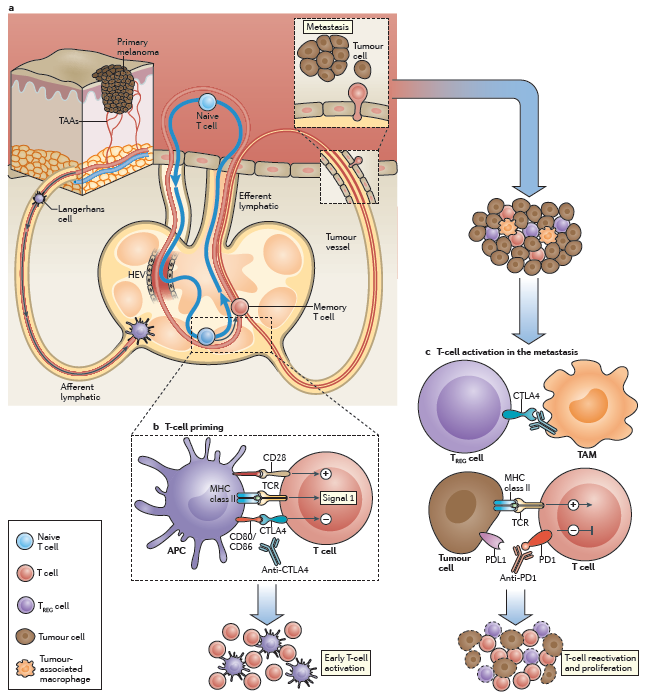
图1:Immune checkpoints and control of T cell activation in melanoma.(来源:Nature Reviews Clinical Oncology)
CTLA-4 和PD-1受体的作用都是调节T细胞活性,但是机制不同。因此,对应的抗体调节T细胞免疫响应的程度也不同(图1)。
CTLA-4是在T细胞上表达的免疫检查点受体。它的激活主要会抑制淋巴组织中T细胞活化早期阶段的免疫响应。此外,CTLA-4还在调节性T细胞(TREG)中表达。这是一种在肿瘤微环境中抑制免疫响应的T细胞。因此,阻断CTLA-4会导致广泛的、非特异性的免疫响应激活。这种对免疫系统广泛的激活作用解释了CTLA-4抗体为何会引发多种不良反应。
与CTLA-4不同,PD-1主要在周围组织(peripheral tissues)和肿瘤微环境中与它的配体相互作用。PD-1有两个配体:PD-L1和 PD-L2。PD-1抑制剂在肿瘤微环境和组织中靶向T细胞更具特异性。因此,相比阻断CTLA-4,PD-1抗体带来的不良反应更有限。
不良反应
通过对免疫检查点抑制剂临床试验的研究,作者们发现,它们可能会在任何组织、器官或系统中导致免疫介导的不良反应。PD-1和CTLA-4抑制剂的副作用通常发生在皮肤、胃肠道、肝脏和内分泌系统,包括瘙痒、皮疹、恶心、腹泻和甲状腺疾病。
这一综述详细汇总了CTLA-4抗体的毒性反应,重点介绍了小肠结肠炎和/或腹泻、皮肤和内分泌相关反应。此外,还分别介绍了PD-1抗体pembrolizumab、nivolumab以及ipilimumab与nivolumab联合疗法的毒性作用(图2、图3)。
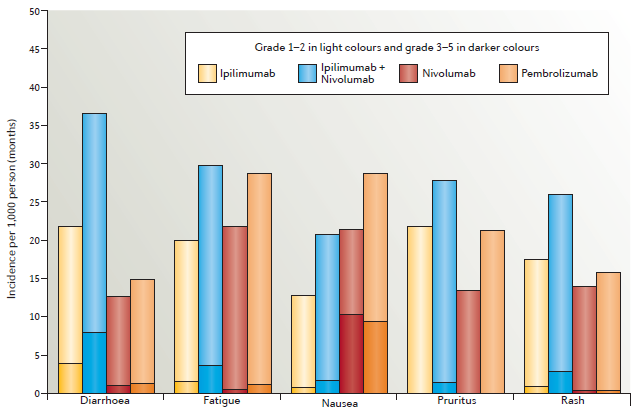
图2:The most common adverse events in patients treated with ipilimumab, pembrolizumab, nivolumab, or ipilimumab plus nivolumab.(来源:Nature Reviews Clinical Oncology)
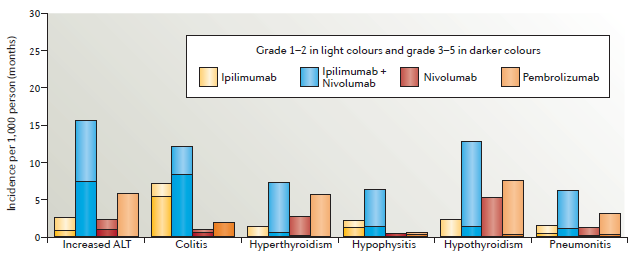
图3:Adverse events of special interest noted with immune-checkpoint inhibitors. (来源:Nature Reviews Clinical Oncology)
如何管理
与其它抗癌药不同的是,检查点抑制剂靶向的是免疫系统,而不是肿瘤。文章表示,这些由免疫检查点抑制剂治疗带来的irAEs通常可以根据经验进行管理,且教育和沟通是成功管理患者的关键因素。
肿瘤专家们需要对这些毒性作用背后的潜在机制有很好的了解。此外,借助一些其它领域的专家(如胃肠病学家、肝脏病学家、内分泌学家、神经学家或皮肤科医生)来管理这些特殊的副作用也是可以考虑的。当然,病人教育也是必不可少的。
据悉,FDA Risk Evaluation and Mitigation Strategy已经提出了ipilimumab引发的irAEs的管理指导方针。作者们认为,pembrolizumab、nivolumab以及联合治疗的副作用的管理也需要相似的指导方针。
一般来说,不干扰日常生活能力的1-2级不良反应是进行对症管理,通常不需要降低剂量或停止治疗(图4)。文章重点介绍了皮肤疾病、胃肠道功能紊乱以及内分泌失调的管理策略。
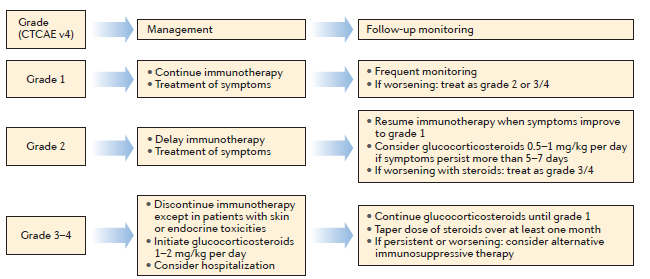
图4:Management of immune-related adverse events excluding skin and endocrine toxicities.(来源:Nature Reviews Clinical Oncology)
附注:靶向CTLA‑4和PD‑1的检查点抑制剂引发的免疫相关不良事件管理指导方针。
结论
检查点抑制剂的使用带来的不良反应与它们的抗肿瘤机制有关。医生应该认识到这一类革命性药物的安全性概况。目前,还有很多问题需要进一步探索,比如,如何实现对这些不良反应的最佳管理。未来的研究应该聚焦如何通过鉴定生物标志物(用于预测治疗响应或者严重的自体免疫毒性风险)优化这些新药的使用。